Neu in der Berg- und Expeditionsmedizin
 Berg- und Expeditionsmedizin
Berg- und Expeditionsmedizin
Die Berg- und Expeditionsmedizin hat in den vergangenen Jahren weltweit immer mehr an Bedeutung gewonnen. Stetig steigt die Anzahl derer, die es in die höchstgelegenen Regionen der Erde zieht. Nach Aufstieg in Höhen über 2.000 bis 2.500 m besteht das Risiko, eine akute Höhenkrankheit zu erleiden. Auch das Risiko für Erkrankungen, die auf einen Sauerstoffmangel zurückzuführen sind, ist in diesen Höhen gesteigert. Hinzu kommt bei entsprechenden Wetterbedingungen das Risiko für Erfrierungen und Unterkühlung. Deutschsprachige Fachgesellschaften, bei denen weiterführende Informationen aus dem Bereich der Gebirgs- und Höhenmedizin eingeholt werden können, stellen die Deutsche Gesellschaft für Berg- und Expeditionsmedizin, die Österreichische Gesellschaft für Alpin- und Höhenmedizin, sowie die Schweizerische Gesellschaft für Gebirgsmedizin dar.
Fallbeispiel 1: Verdacht auf Höhenhirnödem (HHÖ)
Eine 52-jährige gesunde Frau, die auf Meereshöhe lebt, kommt nach einer Tagesreise in ihrem Hotel auf 4.000 m an, nachdem sie den ganzen Tag unterwegs war. Dies ist ihr erster Aufenthalt in einer Höhe über 2.500 m. Abends fühlt sie sich ungewöhnlich erschöpft, leidet unter Kopfschmerzen, Appetitlosigkeit und Übelkeit. Die Einnahme eines Abendessens ist ihr nicht möglich. Am nächsten Morgen klagt sie über stärkste Kopfschmerzen (9/10 Punkte auf der visuellen Analogskala), zusätzlich imponieren Gleichgewichtsstörungen. Die mittels Fingerclip gemessene Sauerstoffsättigung beträgt 73 Prozent. Ein hinzugezogener Mediziner verabreicht ihr Sauerstoff (2 l/min.). Bei Verdacht auf ein beginnendes HHÖ injiziert er zusätzlich Dexamethason (8 mg intramuskulär, gefolgt von 4 mg nach 6 Stunden). Gleichzeitig wird ein Abtransport ins Flachland mittels Helikopter organisiert. Bei fehlenden pulmonalen Rasselgeräuschen wird ein Höhenlungenödem (HLÖ) ausgeschlossen. Bereits wenige Stunden nach Ankunft im Tal sind die Ataxie und Kopfschmerzen verschwunden. Die Patientin erholt sich über Nacht und ist am nächsten Tag beschwerdefrei.
Prävention der akuten Höhenkrankheit
Die akute Höhenkrankheit umfasst drei eigenständige Krankheitsentitäten: Die akute Bergkrankheit (ABK), das Höhenhirnödem (HHÖ) und das Höhenlungenödem (HLÖ). Alle drei Krankheitsbilder können allein oder in Kombination miteinander auftreten. Sie entstehen, wenn bei unzureichender Akklimatisation zu schnell in Höhen von über 2.000 bis 2.500 m aufgestiegen wird [1].
Die wichtigsten Risikofaktoren für die Entstehung aller drei Formen der akuten Höhenkrankheit sind:
• die absolut erreichte Höhe
• die Geschwindigkeit, in der der Höhenunterschied entsteht
• das Ausmaß der Vorakklimatisation
• die individuelle Anfälligkeit.
Entgegen häufiger Annahmen spielen das Geschlecht und die körperliche Leistungsfähigkeit nur eine untergeordnete Rolle [2].
Die Pathophysiologie der ABK ist komplex und nicht vollständig verstanden. Im Zentrum des Krankheitsgeschehens steht die Hypoxämie, die vermutlich über verschiedene Mechanismen (Zunahme der Hirndurchblutung, der zerebralen Gefäßwandpermeabilität sowie des intrakraniellen Drucks) zu einer Aktivierung des trigeminovaskulären Systems führt. Eine ausführlichere Beschreibung des aktuellen pathophysiologischen Verständnisses der ABK findet sich bei [1].
Die ABK äußert sich in Kopfschmerzen, die meist in Kombination mit zumindest einem der folgenden Symptome auftreten: Appetitlosigkeit, Übelkeit, Erbrechen, Schwindel und Abgeschlagenheit [3]. Das HHÖ ist durch Ataxie und Bewusstseinstrübung gekennzeichnet, die in der Regel – aber nicht zwingend – aus einer vorbestehenden ABK hervorgehen. Typische Zeichen eines HLÖ sind ein inadäquater Leistungsabfall, Belastungsdyspnoe sowie ein trockener Husten unter Belastung. Im weiteren Verlauf kommen Ruhedyspnoe, pulmonale Rasselgeräusche, Zyanose, Husten in Ruhe und ein pinkfarbenes, schaumiges Sekret hinzu [4]. Die ABK ist in der Regel selbstlimitierend, wohingegen das HHÖ und HLÖ lebensbedrohliche Erkrankungen darstellen, die einer sofortigen Therapie bedürfen.
Im Zentrum der Prävention der akuten Höhenkrankheit stehen nicht-medikamentöse Verhaltensregeln. Ab einer Höhe von 3.000 m sollte die tägliche Schlafhöhe um nicht mehr als 500 Höhenmeter gesteigert werden [5]. Zusätzlich sollte alle drei bis vier Tage ein Ruhetag eingelegt werden. Werden innerhalb von zwei Monaten vor der Hochtour mehr als fünf Tage auf über 3.000 m
Höhe verbracht, wird das Risiko einer akuten Höhenkrankheit ebenfalls um etwa 50 Prozent reduziert [2].
Liegt eine erhöhte Anfälligkeit für die akute Höhenkrankheit vor und ist ein langsamer Aufstieg nicht möglich oder wirksam, so kann eine medikamentöse Prophylaxe erfolgen. Das Mittel der Wahl zur Prävention der ABK ist Acetazolamid [5]. Bei Vorliegen von Kontraindikationen gegen Acetazolamid kann die Gabe von Dexamethason erwogen werden [5]. Zur medikamentösen Prävention des HLÖ stellt Nifedipin das Mittel der Wahl dar [5]. Wenn dieses nicht eingenommen werden kann, stehen alternativ die Phosphodiestersase-Inhibitoren Tadalafil bzw. Sildenafil zur Verfügung [5]. Tabelle 1 fasst die Empfehlungen und Dosierungen zur medikamentösen Prophylaxe (und Therapie) der akuten Höhenkrankheit zusammen.
Therapie der akuten Höhenkrankheit
Zur Therapie einer leichten ABK reicht meist ein Ruhetag auf gleicher Höhe aus. Kopfschmerzen können durch Schmerzmittel therapiert werden [4]. Bei starker ABK oder wenn die vorgenannten Maßnahmen nicht wirken, können Acetazolamid bzw. Dexamethason gegeben werden und/oder sollte ein Abstieg um 500 bis 1.000 Höhenmeter erfolgen [5]. Ist dies nicht möglich, sollte Sauerstoff verabreicht werden. Wenn die Gegebenheiten einen Abstieg oder die Gabe von Sauerstoff nicht erlauben, kann mit einem portablen Überdrucksack ein Abstieg um über 1.000 Höhenmeter simuliert werden.
Treten Symptome des HLÖ auf, muss so schnell wie möglich abgestiegen werden. Ist nur ein verzögerter Abstieg möglich, sollte unverzüglich Sauerstoff gegeben werden [5]. Mittels eines portablen Überdrucksacks kann als überbrückende Maßnahme ein Abstieg simuliert werden. Zusätzlich sollte Nifedipin gegeben werden [5]. Alternativ kann die Gabe der pulmonalen Vasodilatatoren Sildenafil und Tadalafil erwogen werden (Tabelle 1).
Transportable Überdrucksäcke bestehen aus einem widerstandsfähigen, zylinderförmigen Polyamid-Sack mit etwas über zwei Meter Länge. Die/der Erkrankte wird in den Sack gelegt, der anschließend luftdicht verschlossen wird. Mittels einer hand- oder fußbetriebenen Pumpe wird der Kammerinnendruck (je nach Modell) auf ca. 140 bis 220 mbar gesteigert, was einem simulierten Abstieg um bis zu 2.500 m entspricht. Wegen des mit zunehmender Höhe abnehmenden Luftdrucks ist der durch den Überdruck simulierte „Abstieg“ umso größer, je höher man sich mit dem Überdrucksack befindet. Erkrankte verbleiben meist für einige Stunden im Sack und sollten begleitend Medikamente gegen die akute Höhenkrankheit erhalten (Abbildung 1).
Fallbeispiel 2: Erfrierungen
Im Hochwinter begibt sich ein 50-jähriger Skitourengeher auf eine alpine Tour. Beim Aufstieg wird er von einer Lawine erfasst und verschüttet. Glücklicherweise gibt es eine Atemhöhle, der Tourengeher ist bei Bewusstsein. Während der Verschüttung gelingt es dem Mann eine Hand auszustrecken, diese ragt aus dem Schnee hervor. Einen Handschuh trägt er nicht. Nach 23 Stunden kann der Mann lebend aus der Lawine befreit werden [6].
Falldiskussion Erfrierungen
Die prolongierte Exposition ungeschützter Hautareale und der Akren bei Umgebungstemperaturen unter null Grad Celsius (°C) begünstigt die Entstehung lokaler Erfrierungen [7]. Je länger und kälter die Exposition ist, desto gravierender die Schädigungen.
Erfrierungen werden bei Bergsteigenden insbesondere in großen und extremen Höhen gesichtet. Unangepasste oder nasse Bekleidung, Alkohol- oder Drogenkonsum, keine Unterschlupf- oder Biwakmöglichkeit bei Temperaturen unter null Grad Celsius sind oft mit verantwortlich. Vorerkrankungen wie Gefäßpathologien, Malnutrition, Raynaud-Syndrom, Diabetes mellitus oder Nikotinkonsum können den Gewebeschaden bei Erfrierungen zusätzlich augmentieren.
Spätfolgen von Erfrierungen können Funktionsdefizite bis zum Gewebsverlust und Amputation, chronische Schmerzen, Neuropathien, psychologische Traumata und persistierende Überempfindlichkeit gegenüber Kälte beinhalten. Ca. zwei Drittel der Patienten mit Erfrierungen sind von Langzeitschädigungen betroffen [8].
Pathophysiologie
Durch die prolongierte Kälteexposition kommt es in den exponierten Arealen zu einer Vasokonstriktion mit ischämischer Gewebsschädigung. Der verminderte Blutfluss verhindert den Wärmetransport. Es kommt zu einer Stase mit Formation von Eiskristallen. Diese begünstigen Schädigungen auf mikrovaskulärer und zellulärer Ebene, was zu Inflammation, Ödem, Thrombosen und Zelltod führen kann [9]. In Folge können Nekrosen entstehen. Der Hautschutz wird durch Blasenbildung und Verletzung der Hautbarriere gebrochen, wodurch das Risiko für Infektionen und Dehydrierung ansteigt. Dies ist besonders in abgelegenen Regionen, beispielsweise beim Höhentrekking oder Expeditionen der Fall, wenn ein Abtransport ins Basislager oder ein Aufsuchen einer medizinischen Versorgungsstelle erst verzögert möglich ist (Abbildung 2).
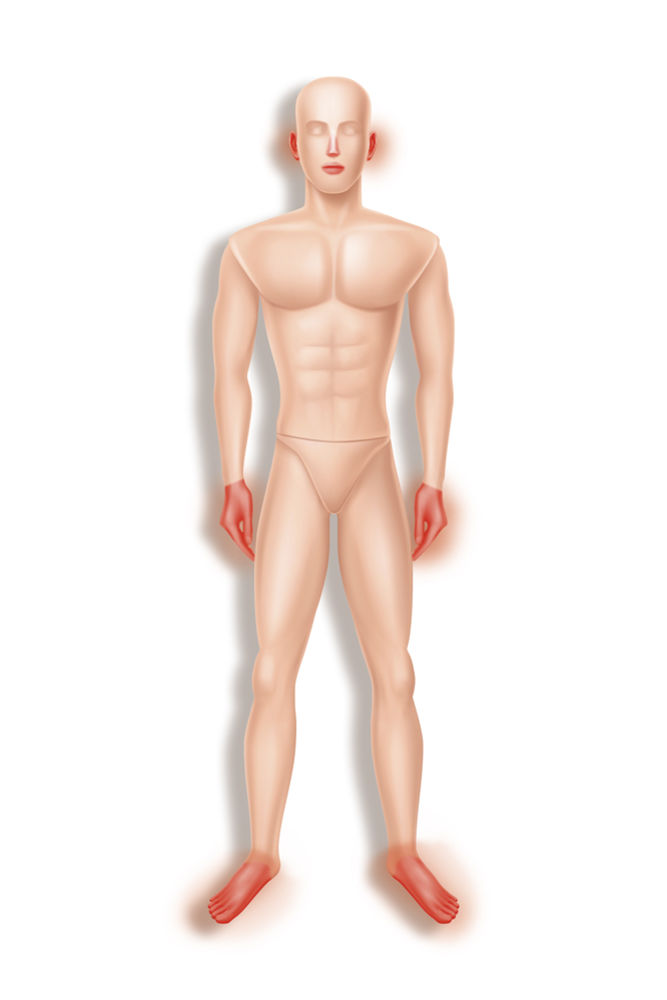
Abbildung 2: Prädilektionsstellen für Erfrierungen sind die Füße (47 %), Hände (19 %), Lippen, Nase und Ohren (3 %) sowie alle exponierten Hautareale.
Vorsicht vor Auftauen und Wiedereinfrieren
Bei einer Erfrierung und dem anschließendem Auftauen des gefrorenen Gewebes werden zellschädigende Mediatoren freigesetzt. Dieser sogenannte Reperfusionsschaden verschlimmert sich, wenn das aufgetaute Gewebe noch einmal einfriert und erneut aufgetaut wird. Dies sollte unbedingt vermieden werden.
Die klinische Präsentation von Erfrierungen kann besonders in der Anfangsphase variieren, und wenig Aussage über die endgültige Schädigung geben. Diese ist oft erst nach Tagen, Wochen oder Monaten eindeutig. Bildgebende Verfahren können helfen, frühzeitig eine Prognose zu stellen [10, 11, 12]. Am gebräuchlichsten für die Schweregradeinteilung und Prognose der Erfrierungen ist aktuell die Einteilung nach Cauchy [13] in vier Stufen (Abbildung 3).
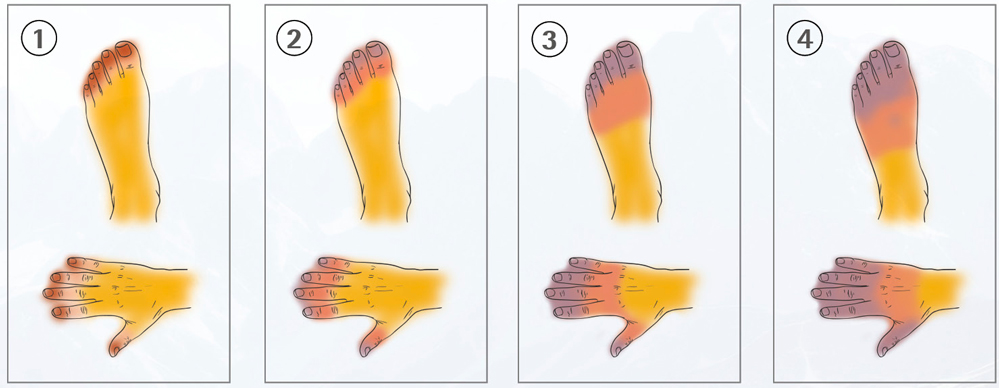
Abbildung 3: Klinische Präsentation der Erfrierungen nach Cauchy.
Therapie von Erfrierungen
Therapieziel ist der Erhalt von möglichst viel intaktem Gewebe, um langfristig eine gute Funktion zu erreichen. Zunächst stehen der Schutz der betroffenen Areale vor weiterer Kälte und Trauma sowie ein rasches Auftauen des Gewebes im Vordergrund. Das Auftauen kann extrem schmerzhaft sein und sollte analgetisch abgedeckt werden. Im Vordergrund der pharmakologischen Therapie steht die Reperfusion des Gewebes durch Vasodilatanzien (Prostacyclin PGI2 Analogon Iloprost) und Thrombolytika (rekombinanter Gewebeplasminogenaktivator –rtPA). Chirurgische Interventionen werden meist erst im Verlauf relevant und sollten durch ein interdisziplinäres, auf Erfrierungen spezialisiertes Team, erfolgen.
In der Vergangenheit durchgeführte Maßnahmen wie eine prophylaktische systemische Antibiotikatherapie oder additiver Sauerstoff werden nicht mehr empfohlen, da sich kein Benefit gezeigt hat [24].
Ergebnis des Fallbeispiels 2
Die Hand des Patienten aus der Lawine konnte erfreulicherweise ohne Gewebeverlust gerettet werden und ist wieder funktionsfähig. Nach zehn Monaten werden noch eine Nageldystrophie sowie Hypästhesien und Hypersensitivität bei Temperaturen unter 14 °C beschrieben. Ebenfalls wird der neuropathische Schmerz (mit Pregabalin) behandelt. Der Patient kann sich bereits wieder sportlich betätigen (Radfahren und Bergsteigen) [25]. Diese eindrückliche Verlaufsdokumentation der Hand zeigt die verschiedenen Stadien des Regenerationsprozesses und das sehr gute Ergebnis (Abbildung 4).
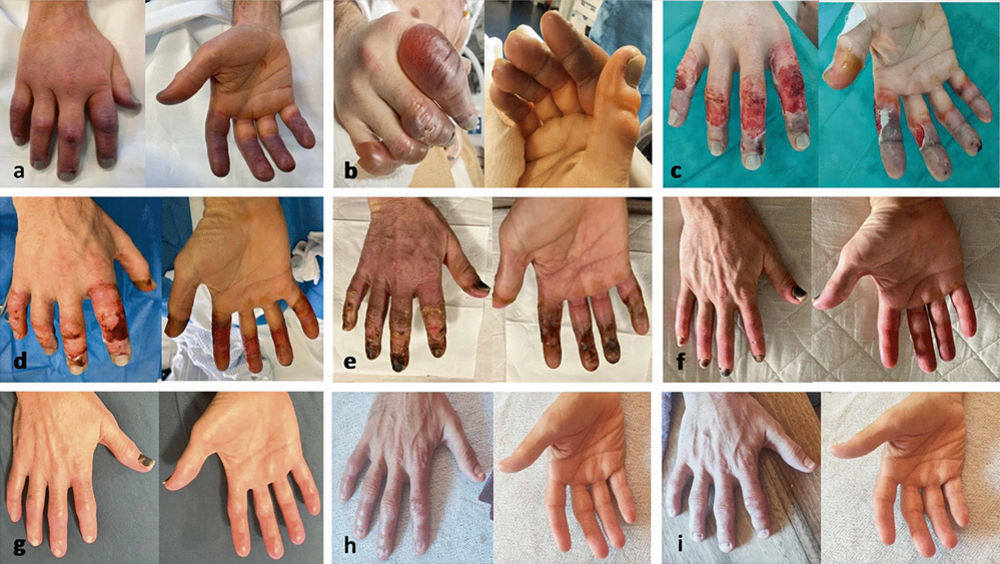
Abbildung 4: Progression der Erfrierungen der rechten Hand. a = Tag 1 nach Wiedererwärmung auf 36 °C Körperkerntemperatur (KKT), b = Tag 4, c = Tag 7, d = Tag 10, e = Tag 27, f = Tag 49, g = 3 Monate, h = 5 Monate, i = 10 Monate. Abbildung entnommen von [6].
Fallbeispiel 3 Hypothermie
Eine 24-jährige Schneeschuhwanderin unternimmt eine winterliche Bergtour. Bei der Querung einer Schneebrücke bricht diese ein, sie stürzt ca. zwei Meter tief in ein darunter liegendes Bachbett mit Eiswasser. Ihr rechtes Bein wird unter einem Fels eingeklemmt, sie kann sich nicht mehr selbst befreien. Ansonsten ist sie unverletzt. Ihr Begleiter muss ca. 20 Minuten absteigen, um die örtliche Bergrettung zu alarmieren.
Als der Begleiter bei der Patientin eintrifft, reagiert diese nur noch verzögert auf seine Rufe. Beim Eintreffen der Bergretter ist die Patientin bewusstlos. Eine epitympanale Temperaturmessung zeigt eine Körperkerntemperatur (KKT) von 25 °C an. Die Patientin zeigt einen schwachen Spontankreislauf mit fünf Atemzügen pro Minute, reagiert aber nicht mehr auf Ansprache oder Schmerzreiz. Defibrillationselektroden werden aufgeklebt, und die Patientin wird unter Monitorkontrolle und in ständiger Reanimationsbereitschaft vorsichtig aus dem Bachbett in einen vorbereiteten, gewärmten Bergesack verbracht.
Falldiskussion Akzidentielle Hypothermie [14]
Hypothermie beginnt ab einer KKT von unter 35 °C [14]. Bei einer KKT von 25 °C ist ein vorhandener Spontankreislauf nicht immer zu erwarten [15]. Das Risiko eines hypothermiebedingten Herzkreislaufstillstandes (HKS) steigt ab einer KKT von unter 30 °C bei gesunden jungen Menschen, beziehungsweise unter 32 °C bei älteren oder multimorbiden Patienten.
Eine prolongierte Kälteexposition und Wärmeverlust durch dünne oder nasse Kleidung, Höhenexposition, Dehydrierung, Erschöpfung, Unterzuckerung, Alkohol oder Drogenkonsum begünstigen eine Hypothermie.
Bei der akzidentellen Hypothermie reduzieren sich die Vitalzeichen bis hin zum Kreislaufstillstand. Bei unterkühlten Patienten ist die Kontrolle der Vitalfunktionen mit größter Sorgfalt durchzuführen. So kann der Puls sehr schwach sein, ebenso ist eine Bradykardie oder Bradypnoe mit nur wenigen Atemzügen pro Minute möglich. Vitalparameter sollten vor allem klinisch über eine Minute erhoben werden.
Die Ermittlung der KKT bedarf spezieller Thermometer, für spontanatmende Patienten benötigt man eine epitympanale Messung, bei Patienten mit Endotrachealtubus kann eine ösophageale Temperatursonde eingelegt werden. Die Thermometer müssen in der Lage sein, eine Temperatur bis unter 10 °C zu erfassen. Wie schnell ein Mensch auskühlt, hängt von den Umgebungsfaktoren ab, kann aber in weniger als einer Stunde lebensbedrohlich werden. In der Lawine werden Abkühlungsraten von bis zu 9 °C pro Stunde beschrieben [16], im Eiswasser kann die Abkühlung bis zu 5 °C pro zehn Minuten betragen [17].
Einteilung Hypothermie
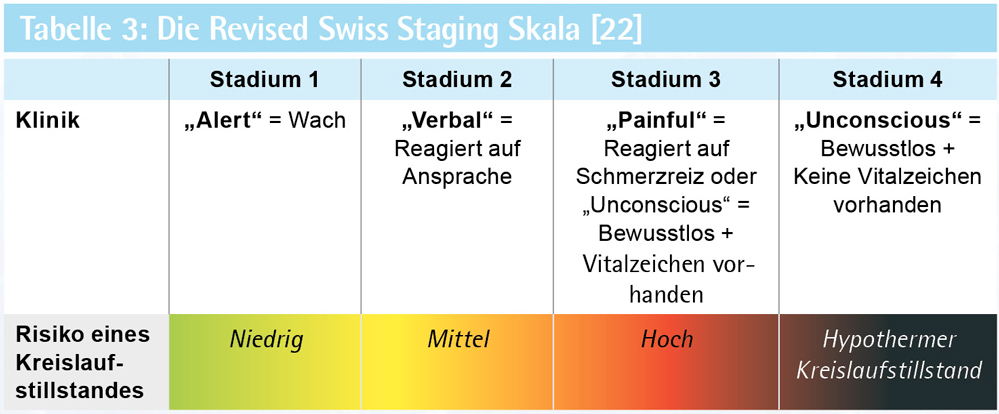
Ein kritischer Aspekt im präklinischen Management von hypothermen Patienten ist die Einschätzung, ob die Patientin/der Patient vital gefährdet ist und ein erhöhtes Risiko trägt, einen hypothermen Kreislaufstillstand zu erleiden. Da eine akkurate Temperaturmessung nicht ubiquitär verfügbar ist, und die Einschätzung der KKT anhand klinischer Parameter schwierig ist, wurde die Schweizer Stadieneinteilung der Hypothermie überarbeitet und das „Revised Swiss Staging“ entwickelt, welches die Vigilanz des Patienten zur Einschätzung einbezieht.
Ein vigilanzgeminderter, hypothermer Patient hat ein hohes Risiko für einen hypothermen Kreislaufstillstand und sollte schonend, aber rasch in eine Klinik zur Wiedererwärmung gebracht werden. Tritt ein hypothermer Kreislaufstillstand ein, haben die Patienten jedoch eine gute Prognose hinsichtlich des neurologischen Outcomes.
Eine Besonderheit im Gebirge und in abgelegenen Gebieten liegt darin, dass es schwierig sein kann, den Patienten gleichzeitig mit hochqualitativer Herzdruckmassage zu versorgen und unter laufender Reanimation abzutransportieren. Ein mechanisches Reanimationsgerät ist in der Bergrettung zunehmend häufiger aber nicht regelhaft verfügbar, insbesondere wenn es sich um eine längere terrestrische Such- und Rettungsaktion handelt. Hier besteht die Möglichkeit, anders als beim normothermen HKS die Reanimation verzögert zu beginnen, beziehungsweise intermittierend fortzuführen. Das reanimationsfreie Intervall wird genutzt, um den Patienten zu transportieren. Dies wird in der Bergrettungsmedizin für steile Passagen mit Abseilstellen, an denen keine manuelle Kardiopulmonale Reanimation (CPR) durchgeführt werden kann oder für Tragepassagen genutzt (Abbildung 5).

Abbildung 5: Algorithmus intermittierende Cardio-Pulmonale Reanimation (iCPR – German Resuscitation Council) PMID: 33773826. CPR = Cardio-Pulmonale Reanimation, HEMS = Helicopter Emergency Medical Service.
Personen mit Vorerkrankungen
Der Anteil der Personen, die mit medizinischen Vorerkrankungen in die Höhe reisen, nimmt immer mehr zu. Während im Jahr 1992 nur etwa 10 Prozent der Trekker in Nepal über 50 Jahre alt waren, lag im Jahr 2016 der Anteil der über 50-Jährigen bei 47 Prozent und der Anteil der über 60-Jährigen bei 15 Prozent Von den Befragten gaben 33 Prozent medizinische Vorerkrankungen an (insbesondere arterielle Hypertonie, Schilddrüsenerkrankungen und Asthma) [23]. Um trotz bestehender Vorerkrankungen sicher in die Höhe reisen zu können, sollte ärztlicherseits evaluiert werden, wie sich eine Abnahme des Luftdrucks und damit des Sauerstoffpartialdrucks in der Umgebungsluft auf den zugrunde liegenden Gesundheitszustand und die Sicherheit einer geplanten Höhenexkursion auswirken.
Eine Reise zu einem hochgelegenen Ziel mag zunächst für viele Personen mit gesundheitlichen Einschränkungen undurchführbar erscheinen. Aber bei sorgfältiger Planung sind Höhenreisen für viele, wenngleich nicht für alle Patienten, möglich. Es wird zwar immer eine Restunsicherheit bezüglich der Höhentoleranz verbleiben, insbesondere bei Reisenden, die sich noch nie in großer Höhe aufgehalten haben. Aber durch gezielte Maßnahmen zur Überwachung des Gesundheitszustands und durch vorheriges Planen, wie auf Veränderungen des Gesundheitszustands zu reagieren ist, lässt sich das Reiserisiko deutlich mindern [23]. Eine vorherige Beratung bei höhenmedizinisch erfahrenen Ärztinnen und Ärzten ist in diesem Falle dringend anzuraten.
Wichtig anzumerken sind die physiologischen Besonderheiten des hypothermen Menschen. Eine Defibrillation bei Kammerflimmern (VF) ist durchaus bei stark unterkühlten Patienten zu erwägen, aufgrund der Hypothermie aber nicht immer erfolgreich. Es sollten bei einer KKT < 30 °C maximal drei Defibrillationsversucheunternommen werden. Sind diese erfolglos, sollte der Patient erst auf > 30 °C KKT wiedererwärmt werden. Es gibt einzelne Fallberichte mit erfolgreichen Defibrillationen bei einer KKT von 25 °C und darunter [18, 19, 20].
Die Wirkung und der Metabolismus der meisten Medikamente sind bei der Hypothermie noch nicht ausreichend bekannt. Eine Adrenalingabe wird bei einer KKT < 30 °C nicht empfohlen. Bei einer KKT zwischen 30 – 35 °C sollte das Dosisintervall auf 6 bis 10 Minuten verlängert werden [21].
Das Wichtigste bei der Hypothermie ist, sie zu erkennen. Hypotherme Patienten mit minimalen Vitalzeichen vermitteln oft einen nicht lebendigen Eindruck. Weite, lichtstarre Pupillen und der Verlust der Hirnstammreflexe oder ein vermeintlicher Rigor Mortis können hypothermiebedingt sein.
Beim Management von hypothermen Patienten gilt äußerste Vorsicht, und der Transport erfolgt unter Reanimationsbereitschaft. Ein beobachteter, hypothermer HKS hat eine gute Prognose.
Das Wichtigste in Kürze
• Alpine Unternehmungen in großen und extremen Höhen erfordern eine sorgfältige Planung, adäquate Ausrüstung und spezielle Kenntnisse in der Bergmedizin. Erkrankungen der Höhe sollten frühzeitig erkannt werden, um die korrekte Therapie
rechtzeitig einzuleiten.
• Die meisten Bergkrankheiten können verhindert oder, wenn früh genug detektiert, gut behandelt werden.
• Vorerkrankungen sind kein Hindernis, aber bedürfen gegebenenfalls zusätzlicher Vorkehrungen.
• Unfälle erfordern zusätzliche Obacht auf die Umgebungsfaktoren in der Höhe, sowie die langen, komplexen oder nicht vorhandenen Rettungsketten.
• Prävention ist ein wichtiger Pfeiler, insbesondere wenn es um Erfrierungen geht.
• Gute Akklimatisation, ordentliche Planung, Kälteschutz und eine angepasste Notfallapotheke sind essenziell für ein gelungenes Bergerlebnis.
Die Autoren erklären, dass sie keine finanziellen oder persönlichen Beziehungen zu Dritten haben, deren Interessen vom Manuskript positiv oder negativ betroffen sein könnten.
Das Literaturverzeichnis kann im Internet unter www.bayerisches-aerzteblatt.de (Aktuelles Heft) abgerufen werden.
Autoren

Professor Dr. Marc Moritz Berger, MBA, DESA 2
1
Klinik für Anästhesie, Intensiv- und Notfallmedizin, Krankenhaus Immenstadt im Klinikverbund Allgäu,
Präsidentin der Deutschen Gesellschaft für Berg- und Expeditionsmedizin (BExMed) sowie Vizepräsidentin der Medizinischen Kommission der Internationalen Kommission für Alpine Rettung (ICAR MEDCOM)
2
Klinik für Anästhesiologie, Intensivmedizin, Notfallmedizin und Schmerztherapie, RKH Klinikum Ludwigsburg sowie Präsidiumsmitglied der Österreichischen Gesellschaft für Alpin- und Höhenmedizin
Teilen:
Das könnte Sie auch interessieren: